Ultrasonido 3D/4D
Acerca de Reseñas Blogs Videos Preguntas y respuestas Dr. Jay Mehta
¿Qué es la ecografía 3d y 4d?
Los exámenes de ultrasonido 3D y 4D le permiten ver a su bebé por nacer con más profundidad y detalle que un ultrasonido 2D estándar. En 3D o 4D, puede ver la imagen real del bebé, es decir, no su órgano interno, sino la piel, la nariz y la lengua. Podrá ver lo que hace su bebé en el útero, como patear, bostezar, etc. En la proyección 2D, los padres pueden ver un color grisáceo desvaído de la imagen en la pantalla. Esta imagen aparece cuando el dispositivo escanea al bebé y muestra sus órganos internos.
Todo lo que necesita saber sobre el ultrasonido 3D/4D
Propósito|Seguridad|Diferencia|Procedimiento|Resultados|Efectos secundarios|Beneficios|Costo
¿Por qué se realizan sonogramas 3D y 4D?
Las madres mayores y aquellas mujeres que pueden tener complicaciones durante el embarazo suelen optar por ecografías 3D y 4D.
El practicante generalmente realiza sonogramas 2D para averiguar si hay alguna anormalidad con el embarazo. Sirven una prueba 2D para examinar el líquido amniótico, la posición del feto y cualquier discapacidad congénita.
Los ecogramas 3D y 4D examinan de cerca las anormalidades fetales. Pueden registrar problemas de labios hendidos y columnas o analizar cualquier otro defecto.
Puede realizar un ultrasonido para los siguientes fines:
– Descubrir su fecha de vencimiento de embarazo. – Monitorear la salud de su bebé. – Confirmar que el embarazo es normal y no es un embarazo ectópico en el que el bebé crece en el tubo de Falopio. – Encontrar la posición del bebé, ya sea que se enfrente a la manera correcta. – Mirando si hay una posibilidad de embarazos múltiples. – Medir el tamaño del feto y la placenta. – Determinar el sexo del bebé. – Verificar el nivel de líquido amniótico alrededor del bebé.
¿Qué es un ultrasonido 3D en el embarazo?
En el ultrasonido 3D, el ecografista graba varias imágenes bidimensionales registradas desde varios ángulos y luego las fusiona para crear una imagen tridimensional. Por ejemplo, podrá ver a su bebé en 3D, como una imagen normal en el teléfono o la computadora portátil. Podrás ver su cara y toda la superficie.
¿Qué es una ecografía 4D en el embarazo?
El Ultrasonido 4D es lo mismo que el Ultrasonido 3D, pero aquí no solo verás la imagen de tu bebé, sino que podrás ver su video. Por lo tanto, en 4D Ultrasound, podrá ver lo que está haciendo su bebé en tiempo real. Puede ver su acción claramente en el monitor a medida que el bebé se mueve o gira.
La seguridad de las ecografías 3D y 4D durante el embarazo
Hacerse una ecografía 3D o 4D es muy tentador ya que podrá ver a sus pequeños. Pero según lo recomendado por el Colegio Estadounidense de Obstetras y Ginecólogos (ACOG), el ultrasonido siempre debe realizarse con fines médicos. El procedimiento es seguro tanto para el bebé como para la madre. Aunque no implica ningún riesgo, sin embargo, es recomendable realizarlo solo cuando sea necesario y por un médico calificado.
Cuando realizas Ultrasonido, transmite algo de calor en el tejido; por lo tanto, crean pequeñas burbujas de gas en los tejidos y fluidos corporales. Este calentamiento puede dañar su cuerpo a largo plazo. ACOG también recomienda que las mujeres se sometan a una prueba de ultrasonido 2D entre las semanas 18 y 22 de embarazo.
Diferencia entre ecografías 2D, Doppler, 3D y 4D
Para comprender la diferencia entre los diferentes tipos de ultrasonido, debe observar su procedimiento:
Ultrasonido 2D: para este método, el médico usa un dispositivo transductor para enviar ondas de sonido en su cuerpo. Cuando el transductor se presiona contra la piel o se coloca en la vagina, envía ondas que golpean los órganos o fluidos internos y rebotan. Esta onda que rebota crea un eco, lo que ayuda a crear una imagen en el monitor. Esta imagen es una vista transversal donde se puede ver un contorno grisáceo del bebé.
Ultrasonido Doppler: Doppler es un tipo de ultrasonido que ayuda a escuchar los latidos del corazón del bebé o el flujo de sangre a través del cuerpo. El radiólogo usa un dispositivo manual, que frota con un gel especial que se aplica en el área abdominal para escuchar los latidos del corazón del feto.
Ultrasonido 3D: En este método verás con mayor claridad la imagen del bebé. Crea una imagen tridimensional del bebé al registrar los detalles internos y externos de los órganos desde diferentes ángulos. En el monitor, podrá ver el corazón, los vasos sanguíneos o las válvulas del feto, la piel, la boca o la forma del bebé.
Ultrasonido 4D: 4D es similar a 3D; la diferencia más significativa es que por Ultrasonido 4D, podrás ver el video en vivo de tu bebé. El ultrasonido puede registrar el movimiento lineal del bebé, como cuando el bebé mueve las manos o las piernas o bosteza.
¿Como funciona?
En Ultrasonido 2D, envían ondas de sonido y reflejos del cuerpo para registrar su eco. El transductor interpreta este eco para formar una imagen visual del bebé.
El ultrasonido 3D es algo similar al ultrasonido 2D, solo que registran las ondas desde múltiples ángulos. Los médicos convierten múltiples imágenes producidas desde diferentes ángulos en una sola a través de un software sofisticado. Este tipo de proceso de algoritmo de ultrasonido crea imágenes, que también se conocen como “representación de superficie”.. Este software produce una representación precisa del feto y la muestra en el monitor. Estas increíbles imágenes muestran una imagen detallada del cuerpo y la cara del bebé.
El proceso de ultrasonido 4D es de la misma manera, pero las imágenes se mueven o se capturan por segundo. Entonces, el monitor muestra un video en lugar de una imagen fija del bebé.
¿Quién se hace la prueba?
Las mujeres que tienen un bajo riesgo de sufrir alguna complicación pasan por el proceso de ultrasonido solo una vez. Sin embargo, aquellas mujeres que tienen riesgo de tener dificultades o posibilidades de concebir partos múltiples suelen realizar más pruebas. Puede haber muchas razones para hacerse la prueba según el trimestre. No obstante, las ecografías 3D y 4D son opcionales.
¿Qué hace la prueba?
Al igual que los ultrasonidos 2D regulares, los ultrasonidos 3D y 4D también crean imágenes al registrar las ondas sonoras. Pero aquí, la imagen producida es una imagen tridimensional del bebé. Y si es una ecografía 4D, no cambiará una imagen fija; se convertirá en un video.
¿Cómo se hace la prueba?
Si va a realizarse una ecografía abdominal, el médico le pedirá que se acueste y le frotará un poco de gel a base de agua en la barriga. Este gel ayuda a transferir las ondas del transductor al cuerpo y devolverlas. El médico moverá el dispositivo hacia adelante y hacia atrás para crear la imagen de su bebé en la pantalla.
¿Qué saber sobre los resultados de las pruebas?
Una vez finalizada la prueba, obtendrá una foto o una copia en video del bebé para llevarla a casa. El médico le indicará si hay algún defecto o si necesita tomar algunas precauciones.
Asegúrese de realizar la prueba solo en un centro médico por un médico calificado y experimentado. La ecografía en un local comercial no sustituye al centro médico.
Efectos secundarios de los ultrasonidos 3D y 4D
Aunque no se conocen efectos secundarios del proceso, a veces calienta un poco el tejido. Este calentamiento del tejido crea bolsas de gas dentro del tejido. Por lo que es recomendable realizar la actividad de ultrasonido solo cuando lo solicite el médico. No hay investigaciones en los últimos veinte años que sugieran que crea algún daño a la madre o al bebé, pero debe evitarlo si es posible.
El médico recomienda realizarse una ecografía 3D o 4D entre la semana 26 y 34 del período de embarazo. Sin embargo, también podrá obtener una imagen clara del bebé en cualquier momento después de 24 semanas de haberlo concebido.
Los beneficios de la ecografía 3D/4D Baby
Los siguientes son los beneficios del proceso:
– Podrás ver la imagen en vivo de la piel, la boca o toda la superficie de tu bebé. – Puedes controlar el tamaño del bebé. – Evaluar su movimiento. – Confirmar la fecha de vencimiento.
Costo de Ultrasonido 3D y 4D
Pasar por el proceso es relativamente barato; puede oscilar entre Rs 750 y Rs 3000.
Reseñas de Google
Nikhil Mehra
Uno de los mejores especialistas en FIV y centro de atención ginecológica avanzada. El médico con más conocimientos y experiencia que se preocupa por sus pacientes y garantiza el mejor tratamiento. La clínica Shree IVF tiene instalaciones de clase mundial disponibles bajo un mismo techo. Muchas tecnologías se agregaron por primera vez en India. Lo recomiendo encarecidamente a todo el mundo.
Shilpa Patwardhan
Dr. Jay Sir es una persona muy inteligente y sabia. Es un todoterreno con excelentes capacidades de tutoría, lo que significa que no solo trabaja, sino que también guía, enseña, brinda observaciones de primera mano, brinda oportunidades para aprender y crecer como médico, con demostraciones quirúrgicas prácticas en vivo. Demuestra un significado literal del término “Los médicos son mensajeros de Dios”, he observado sus puntos de vista imparciales y su respeto hacia todas las demás patologías.
Shefali Parekh
El Dr. Jay Mehta es un excelente especialista en FIV. Él y su maravilloso equipo son responsables de los excelentes resultados aquí. Lo bueno es que el Dr. Jay toma él mismo la recolección de óvulos y la transferencia de embriones para todos los pacientes. Son muy buenos con la asesoría financiera del procedimiento. El costo casi nunca aumentará. Estamos muy contentos con los servicios del local.
Swadha Kotpalliwar
El Dr. Jay es definitivamente uno de los mejores cirujanos laparoscópicos y especialistas en fiv. Sus cirugías son un placer para muchos ginecólogos. Amable de corazón y sus enseñanzas son valiosas, ¡uno no puede perderse!
Nikhil Mehra
Uno de los mejores especialistas en FIV y centro de atención ginecológica avanzada. El médico con más conocimientos y experiencia que se preocupa por sus pacientes y garantiza el mejor tratamiento. La clínica Shree IVF tiene instalaciones de clase mundial disponibles bajo un mismo techo. Muchas tecnologías se agregaron por primera vez en India. Lo recomiendo encarecidamente a todo el mundo.
Shilpa Patwardhan
El Dr. Jay Sir es una persona muy inteligente y sabia. Es un todoterreno con excelentes capacidades de tutoría, lo que significa que no solo trabaja, sino que también guía, enseña, brinda observaciones de primera mano, brinda oportunidades para aprender y crecer como médico, con demostraciones quirúrgicas prácticas en vivo. Demuestra un significado literal del término “Los médicos son mensajeros de Dios”, he observado sus puntos de vista imparciales y su respeto hacia todas las demás patologías.
PIROPO #28
El Dr. Jay Mehta es un ser humano maravilloso y un médico increíble. Nunca he visto un médico tan práctico que sea muy transparente en su conversación. Me sometí a una histerectomía laparoscópica hace tres años y me dieron de alta en 24 horas. Hasta la fecha, no tengo ningún problema. Recientemente ingresé a mi suegra, y se está recuperando asombrosamente. Felicitaciones a usted doctor. Te estaré siempre agradecida.
Sandip Chaván
Dr. Jay Mehta es un obstetra, ginecólogo y fetólogo muy profesional, conocedor y dotado de Dios que cree en la autenticidad y las formas éticas de ayudar a las familias por una causa noble. Él es “Salvando generaciones”. Otro esfuerzo interesante, sincero y bastante responsable del Dr. Jay son las conferencias de orientación en línea sobre ginecología y obstetricia para médicos de familia en ejercicio de toda la India. Más bien, ama y disfruta compartir sus mejores experiencias. ¡Que Dios lo bendiga por siempre…!
blogs
Todos los blogs
Video
Todo el vídeo
preguntas y respuestas
Todas las preguntas y respuestas
¡UPS! CONTENIDO NO ENCONTRADO
Dr. jay mehta
Especialista en Fertilidad y FIV
4.9
Verificado y más confiable
El Dr. Jay Mehta es el director científico de Shree IVF Clinic. Es un conocido especialista en Fertilidad y FIV y también uno de los pocos médicos en el país que se especializa en Embriología y Andrología.
 Si tiene una prueba de Papanicolaou anormal y otros síntomas de cáncer de cuello uterino, su ginecólogo querrá saber más sobre su historial médico y el de su familia. Es probable que realicen más pruebas para averiguar si tiene células cancerosas en el cuello uterino y revisarán los ganglios linfáticos para ver si el cáncer se ha propagado.
Si tiene una prueba de Papanicolaou anormal y otros síntomas de cáncer de cuello uterino, su ginecólogo querrá saber más sobre su historial médico y el de su familia. Es probable que realicen más pruebas para averiguar si tiene células cancerosas en el cuello uterino y revisarán los ganglios linfáticos para ver si el cáncer se ha propagado.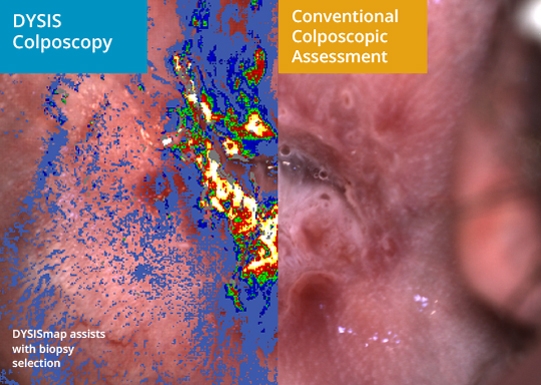 Colposcopia. Durante esta prueba, su médico usará un instrumento llamado colposcopio, que se parece mucho a un microscopio, para observar de cerca su cuello uterino. Te acostarás en una mesa de examen y usarán un espéculo para mantener su vagina abierta.
Colposcopia. Durante esta prueba, su médico usará un instrumento llamado colposcopio, que se parece mucho a un microscopio, para observar de cerca su cuello uterino. Te acostarás en una mesa de examen y usarán un espéculo para mantener su vagina abierta.
 Es posible que se sienta un poco ansiosa después de una colposcopía. Es normal estar preocupado por los resultados de la colposcopía. Antes de irse a casa después de su procedimiento, pregúntele a su médico cuándo puede esperar resultados y cómo se entregarán.
Es posible que se sienta un poco ansiosa después de una colposcopía. Es normal estar preocupado por los resultados de la colposcopía. Antes de irse a casa después de su procedimiento, pregúntele a su médico cuándo puede esperar resultados y cómo se entregarán.


 El análisis temático (AT) fue seleccionado como el método más apropiado para este estudio; es un enfoque que se puede utilizar para identificar, analizar y organizar patrones de opiniones dentro de un conjunto de datos. Elegimos este método porque las experiencias de los participantes se pueden analizar sin evaluar cómo experimentan la realidad (como con IPA o fenomenología). También proporciona la flexibilidad para permitir que los participantes amplíen sus preocupaciones e intereses sin desviarse del proceso de toma de decisiones (que era el objetivo de este estudio). Se eligió TA en lugar de teoría fundamentada, ya que los datos se recopilaron mediante el uso de grupos focales y el enfoque no se centró en los procesos sociales [22, 23]. Los datos se codificaron de forma inductiva, utilizando el proceso TA de seis etapas darticulo por Braun y Clarke [24]; como se describe a continuación.
El análisis temático (AT) fue seleccionado como el método más apropiado para este estudio; es un enfoque que se puede utilizar para identificar, analizar y organizar patrones de opiniones dentro de un conjunto de datos. Elegimos este método porque las experiencias de los participantes se pueden analizar sin evaluar cómo experimentan la realidad (como con IPA o fenomenología). También proporciona la flexibilidad para permitir que los participantes amplíen sus preocupaciones e intereses sin desviarse del proceso de toma de decisiones (que era el objetivo de este estudio). Se eligió TA en lugar de teoría fundamentada, ya que los datos se recopilaron mediante el uso de grupos focales y el enfoque no se centró en los procesos sociales [22, 23]. Los datos se codificaron de forma inductiva, utilizando el proceso TA de seis etapas darticulo por Braun y Clarke [24]; como se describe a continuación. Aquellas que no toman testosterona y que no se han sometido a ninguna cirugía de afirmación de género, como una mastectomía o cirugía superior (extirpación de los senos), o una ooforectomía (extirpación de los ovarios) tienen el mismo riesgo de desarrollar cáncer de mama que las mujeres cisgénero. Gran parte de lo que sabemos sobre los hombres trans y el cáncer de mama se basa en informes de casos (un informe detallado del diagnóstico, tratamiento y seguimiento de una persona, que generalmente se usa para casos poco frecuentes). Debido a que estos informes se basan en personas individuales, es posible que no se puedan generalizar a toda la población y no nos permitan comprender la frecuencia del cáncer de mama entre los hombres trans. Desde principios de la década de 2000, se han informado menos de 20 casos de cáncer de mama en hombres trans en la literatura médica.
Aquellas que no toman testosterona y que no se han sometido a ninguna cirugía de afirmación de género, como una mastectomía o cirugía superior (extirpación de los senos), o una ooforectomía (extirpación de los ovarios) tienen el mismo riesgo de desarrollar cáncer de mama que las mujeres cisgénero. Gran parte de lo que sabemos sobre los hombres trans y el cáncer de mama se basa en informes de casos (un informe detallado del diagnóstico, tratamiento y seguimiento de una persona, que generalmente se usa para casos poco frecuentes). Debido a que estos informes se basan en personas individuales, es posible que no se puedan generalizar a toda la población y no nos permitan comprender la frecuencia del cáncer de mama entre los hombres trans. Desde principios de la década de 2000, se han informado menos de 20 casos de cáncer de mama en hombres trans en la literatura médica.